鲁教版化学课本九年级下册第八单元练习课后答案
1练习第1~5题答案
| 1 | 2 | 3 | 4 | 5 |
| C | C | D | A | C |
2练习第6题答案
(1)24℃
(2)<24℃
(3)不饱和
(4)20g
解析:氯化钠与硝酸钾溶解度曲线的交点对应的横坐标温度为24℃。在小于24℃时,氯化钠的溶解度曲线在硝酸钾溶解度曲线的上方,此时氯化钠的溶解度大于硝酸钾的溶解度。P点在硝酸钾溶解度曲线的下方,所以此点表示硝酸钾的不饱和溶液。通过观察不难发现10℃时硝酸钾的溶解度为20g。
3练习第7题答案
(1)盐酸;氯化钠溶液;使紫色石蕊试液变红的是盐酸,不能使紫色石蕊试液变色的是氯化钠
(2)向另外两支试管中滴加盐酸,有气体产生的是碳酸钠溶液,没有明显现象的是氢氧化钠。
解析:四种溶液中显酸性的是盐酸,显碱性的是NaOH和Na2 C03,显中性的是NaCI,因此用紫色石蕊试液可鉴别出盐酸和NaCI两种溶液,根据Na2 C03与盐酸反应会产生C02,NaOH与盐酸虽然反应但无明显现象的性质可鉴别出NaOH和Na2 C03两种溶液。
4练习第8题答案
(1)如图8-11所示。
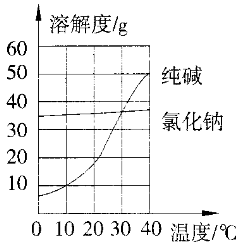
图8-11
(2)纯碱的溶解度受温度变化影响较大,冬天温度低,湖水中会有大量纯碱晶体析出,即降温结晶,再利用过滤的方法捞碱;食盐的溶解度随温度变化不大,夏季温度高,利用高温将湖水蒸发可获得粗盐,而纯碱在高温时溶解度较大,不会析出,利用的是蒸发结品的原理。
解析:绘制溶解度曲线时,先根据不同温度下物质的溶解度进行描点,然后利用平滑的曲线连接起来。
5练习第9题答案


解析:用反应前烧杯中物质的总质量减去反应后烧杯中物质的总质量就是逸出的C02的质量,根据C02的质量可求出Na2 C03的质量,用Na2 C03的质量除以样品的总质量,就可求出样品中纯碱的质量分数。
6练习第10题答案
(1)硫酸铜晶体大小不变,形状发生变化,变为规则形状。
(2)溶液中的硫酸铜析出到晶体表面,而晶体表面的硫酸铜又溶解到溶液中,两者的速率相等,所以晶体的大小没有改变.溶液中的硫酸铜质量也没有改变。
(3)涉及饱和溶液、溶解度、结晶等知识。
解析:本实验中利用的溶液为硫酸铜饱和溶液,当向其中再加入溶质硫酸铜时,晶体表面的硫酸铜会溶解在溶液中,同时溶液中的硫酸铜又析出到晶体表面,溶解和结晶的速率相等,故晶体的大小没有改变,溶液中的硫酸铜的质量也没有增减,但晶体的形状会发生变化。